Ο καρκίνος του μαστού είναι η δεύτερη συχνό-τερη κακοήθεια στις γυναίκες μετά τον καρκίνο του δέρματος 1. To 20-50% των όγκων αυτών εμφανίζει υπερέκφραση του HER2, ενός από τους τέσσερις επιδερμιδικούς υποδοχείς των αυξητικών παραγόντων2 και έχει πολύ χειρό-τερη πρόγνωση3. Η τραστουζουμάμπη είναι ένα εξανθρωπισμένο μονοκλωνικό αντίσωμα που δρα τόσο στο ενδο- όσο και στο εξωκυττάριο τμήμα του HER2 μειώνοντας τη θνητότητα κατά 33% και τις υποτροπές του καρκίνου του μαστού κατά 50%4, 5. Ωστόσο σε αξιοσημείωτο ποσοστό ευθύνεται για την εμφάνιση καρδιοτοξικότητας και η απόφαση για την ιδανική αντιμετώπιση απαιτεί συνεργασία ογκολόγου – καρδιολόγου και παρακολούθηση σε ειδικό καρδιογκολογικό ιατρείο6. Γυναίκα 45 ετών με καρκίνο μαστού παραπέμφθηκε από τους ογκολόγους στο καρδιο-ογκολογικό ιατρείο λόγω α-συμπτωματικής μείωσης του κλάσματος εξωθήσεως (LVEF). Η διάγνωση του καρκίνου στον αριστερό μαστό (στάδιο 1Α), είχε τεθεί πριν 10 μήνες. Πρόκειται για τριπλά θετικό νεόπλασμα [στους υποδοχείς οιστρογόνων (ER+), προγεστερόνης (PR+) και HER2+)] για το οποίο είχε υποβληθεί σε αριστερή μαστεκτομή. Το πρώτο σχήμα που έλαβε περιλάμβανε 4 κύκλους α-δριαμυκίνης (100mg/ κύκλο) και κυκλοφωσφαμίδης (1000mg/κύκλο). Στη συνέχεια χορηγήθηκε πακλιταξέλη (120mg/εβδομάδα) και τραστουζουμάμπη (600mg/3 εβδομάδες) για 12 εβδομάδες, ενώ ακολούθως η ασθενής λάμβανε τραστουζουμάμπη (600mg /3 εβδομάδες), λετροζόλη και τριπτορελίνη.
Από το ατομικό αναμνηστικό σημειώνεται κάπνισμα (30 πακέτα-έτη) και θετικό οικογενειακό ιστορικό πρώιμης στεφανιαίας νόσου, καθώς η αδελφή της υπέστη οξύ έμφραγμα του μυοκαρδίου σε ηλικία 42 ετών. Επιπλέον, η ασθενής ανέφερε και δύο επεισόδια εν τω βάθει φλεβικής θρόμβωσης στα κάτω άκρα – πριν τη διάγνωση της νεοπλασίας του μαστού για τα οποία μετά από διερεύνηση δεν βρέθηκε αιτιολογικός παράγοντας.
Πριν την έναρξη της θεραπείας με τραστουζουμάμπη (600mg/3 εβδομάδες), λετροζόλη και τριπτορελίνη, η ασθενής είχε υποβληθεί σε υπε-ρηχοκαρδιογράφημα σε άλλο εργαστήριο που ανέδειξε φυσιολογική δομή και λειτουργικότητα αμφότερων των κοιλιών με LVEF 62%, ενώ 3 μήνες μετά, το LVEF μειώθηκε στο 52% και για το λόγο αυτό η ασθενής παραπέμφθηκε στο καρδιο-ογκολογικό ιατρείο.
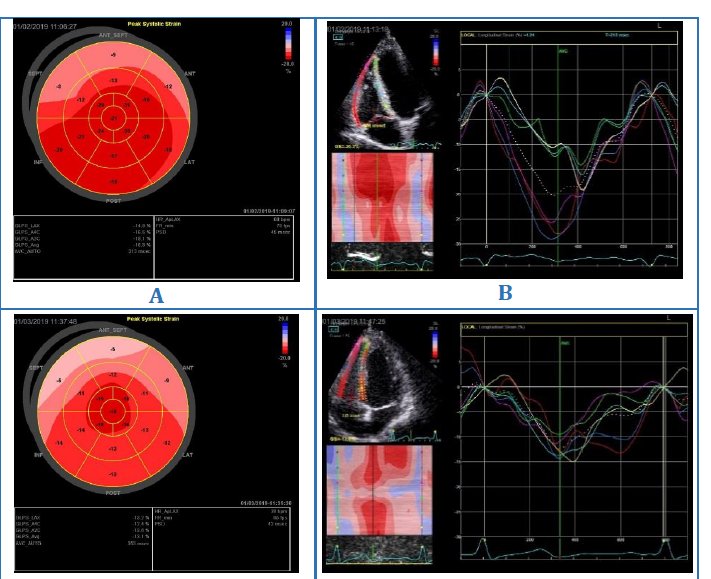
Κατά την κλινική εξέταση η ασθενής είχε ΒΜΙ 19.7kg/m2, ήταν ασυμπτωματική, αιμοδυναμικά σταθερή με αρτηριακή πίεση 130/70mmHg, 96 σφύξεις/λεπτό, SpO2 = 99% και ηλεκτροκαρδιογράφημα με φλεβοκομβικό ρυθμό και αριστερό οπίσθιο ημισκελικό αποκλεισμό. Το υπερηχοκαρδιογράφημα έδειξε διατηρημένη συστολική λειτουργία και των δύο κοιλιών με LVEF 55%, συνολική επιμήκη παραμόρφωση αριστερής κοιλίας (LVGLS) – 16.8% και δεξιάς κοιλίας (RVGLS) – 20.3% (Εικόνες A και Β). Με βάση τα ευρήματα αυτά, συνεστήθη στην ασθενή να ξεκινήσει καρβεδιλόλη σε δόση 3.125mg δύο φορές την ημέρα (b.i.d.) και εναλαπρίλη 2.5mg (b.i.d.) στο πλαίσιο καρδιοπροστασίας, συνεχίζοντας κανονικά την αγωγή της με τραστουζουμάμπη.
Η επηρεασμένη τιμή του LVGLS ήταν ο λόγος για τον οποίο η ασθενής επανεκτιμήθηκε μόλις μετά από 15 μέρες. Παρέμενε ασυμπτωματική, ενώ διαπιστώθηκε περαιτέρω μείωση του LVEF κατά 8 εκατοστιαίες μονάδες (LVEF =47%), καθώς και των δεικτών επιμήκους παραμόρφωσης (LVGLS = – 14.5% και RVGLS = -16.4%). Με βάση τις μετρήσεις αυτές και την αιμοδυναμική της κατάσταση (ΑΠ = 133/101 mmHg, 94 σφύξεις/λεπτό), συναποφασίστηκε με τους θεράποντες ογκολόγους προσωρινή διακοπή της τραστουζουμάμπης, αύξηση της δόσης της καρβεδιλόλης σε 6.125mg (b.i.d.) και της εναλαπρίλης στα 5mg (b.i.d.) και προγραμματίστηκε επανεκτίμηση σε 2 εβδομάδες.
Στην επόμενη επίσκεψη, η κλινική εικόνα της α-σθενούς παρέμενε αμετάβλητη, ενώ σημειώθηκε νέα μείωση όλων των δεικτών συστολικής λειτουργίας (LVEF 41% και LV GLS -13%, RV GLS -12.3%) (Εικόνες Γ και Δ). Συνακόλουθα στην αγωγή της προστέθηκαν 5mg ροσουβαστατίνηs και η δόση της καρβεδιλόλης τιτλοποιήθηκε περαιτέρω στα 12.5mg (b.i.d.) , λαμβάνοντας υπόψη την αρτηριακή της πίεση (ΑΠ= 112/88mmHg) και την καρδιακή της συχνότητα (83 σφύξεις/λεπτό).
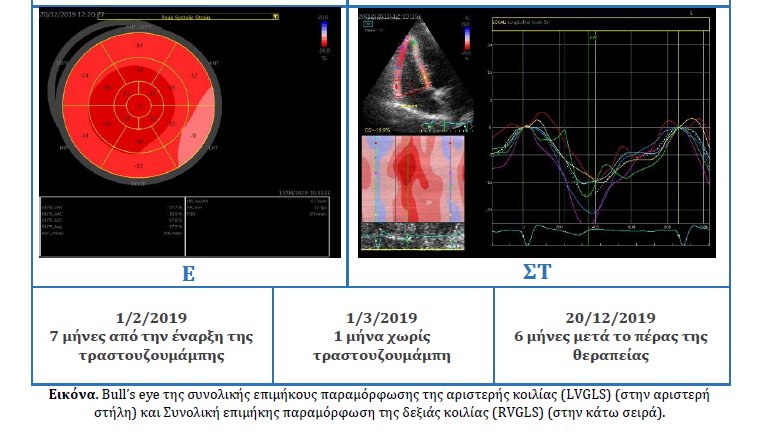
Μετά από δύο ακόμα εβδομάδες χωρίς τραστουζουμάμπη, τόσο το LVEF (50%), όσο και οι δείκτες παραμόρφωσης των κοιλιών (LVGLS -15.4% και RVGLS – 16.8%) άρχισαν να βελτιώνονται. Αποφασίστηκε τότε η επανέναρξη της τραστουζουμάμπης, με προσθήκη 25mg σπιρονολακτόνης. Έναν μήνα αργότερα, η ασθενής παρέμενε σε πολύ καλή γενική κατάσταση, με σταθερό LVEF στο 50%, ενώ οι τιμές της επιμήκους παραμόρφωσης ήταν LV GLS -13.5% και RV GLS – 18.4%. Με τα δεδομένα αυτά, η ασθενής συνέχισε και κατάφερε να ολοκληρώσει επιτυχώς τη θεραπεία της με τραστουζουμάμπη για 12 μήνες υπό στενή καρδιολογική παρακολούθηση. Έξι μήνες μετά το τέλος αυτής, παραμένει ασυμπτωματική με LVEF 50%, LVGLS -17.7% και RVGLS -19.9% (Εικόνες Ε και ΣΤ).
Συζήτηση
Η τραστουζουμάμπη βελτιώνει σημαντικά την πρόγνωση των ασθενών με HER2+ καρκίνο μαστού, αλλά σχετίζεται με 5 πλάσια πιθανότητα ασυμπτωματικής μείωσης του LVEF και 1.8 φορές υψηλότερο κίνδυνο εμφάνισης καρδιακής ανεπάρκειας.7 Έτσι το 10% των ασθενών εμφανίζει ασυμπτωματική μείωση του LVEF4, 8, ενώ το 14% αυτών εμφανίζει καρδιακή ανεπάρκεια9. Ο κίνδυνος είναι πολύ μεγαλύτερος όταν η τραστουζουμάμπη συγχορηγείται με ανθρακυκλίνες,10 ενώ όταν έπεται των ανθρακυκλινών, ο κίνδυνος είναι μετρίως αυξημένος,11 όπως στην περίπτωση της ασθενούς που περιγράφεται.
Στους παράγοντες κινδύνου για την εμφάνιση καρδιοτοξικότητας από τραστουζουμάμπη εκτός από την προηγηθείσα χρήση ανθρακυκλινών συγκαταλέγεται η μεγάλη ηλικία (>65 ετών), η παχυσαρκία (ΒΜΙ≥30kg/m2 ), η προϋπάρχουσα καρδιακή δυσλειτουργία, η υπέρταση, η προηγηθείσα ακτινοθεραπεία και αρχικό LVGLS > -18%.12, 13 Επιπρόσθετα, πρόσφατα μεμονωμένες μελέτες αναγνώρισαν ότι οι τμηματικές διαταραχές κινητικότητας της αριστερής κοιλίας 14 και οι βαλβιδοπάθειες,15 συγκαταλέγονται επίσης στους προγνωστικούς παράγοντες για την ανάπτυξη καρδιοτοξικότητας από την τραστουζουμάμπη.
H ασθενής μας δεν είχε κανένα από τους αναφερόμενους κλασσικούς παράγοντες κινδύνου για καρδιοτοξικότητα, πλην της προηγηθείσας χορήγησης ανθρακυκλινών. Ανεξαρτήτως όμως του αρχικού κινδύνου, όλοι οι ασθενείς που λαμβάνουν τραστουζουμάμπη σύμφωνα τόσο με το SPC (Summary of Product Characteristics –
Περίληψη Χαρακτηριστικών Προϊόντος) του φαρμάκου,16 όσο και με τις σύγχρονες συστάσεις, πρέπει να παρακολουθούνται υπερηχοκαρδιογραφικά με εκτίμηση του LVEF, αλλά και του LVGLS – που υπερέχει στην εκτίμηση της μυοκαρδιακής βλάβης 17, 18 – ανά 3 μήνες μέχρι την ολοκλήρωση της θεραπείας.19 Μάλιστα στις πιο πρόσφατες κατευθυντήριες οδηγίες της Ευρωπαϊκής Εταιρείας Ογκολογίας, αναφέρεται ότι το LVGLS στους ασθενείς αυτούς ανιχνεύει τη μυοκαρδιακή τοξικότητα του φαρμάκου 3 μήνες νωρίτερα από την πτώση του LVEF, παρέχοντας ενδεχομένως αυτό το χρονικό παράθυρο για έναρξη καρδιοπροστατευτικής φαρμακευτικής αγωγής (δηλαδή, αναστολείς του μετατρεπτικού ενζύμου της αγγειοτασίνης ή ανταγωνιστές των υποδοχέων της αγγειοτασίνης ΙΙ ή/και β-αποκλειστές)20. Σε καμία περίπτωση όμως, δε συστήνεται η διακοπή της σωτήριας για τη ζωή του ασθενούς θεραπεία με βάση μόνο τις μεταβολές του strain. Συνακόλουθα, στην περίπτωση της ασθενούς μας που κατά την πρώτη εκτίμηση στο ιατρείο μας μετά την έναρξη της τραστουζουμάμπης διαπιστώθηκε LVGLS– 16.8% με LVEF 55%, συστήσαμε έναρξη καρβεδιλόλης και εναλαπρίλης.
Η δεύτερη θεραπευτική παρέμβαση έλαβε χώρα κατά την ασυμπτωματική μείωση του LVEF στην επόμενη εκτίμηση της ασθενούς (47% από 62% αρχικά), που πληρούσε τα κριτήρια της καρδιοτοξικότητας (μείωση του LVEF ≥10%
από την αρχική τιμή και <50%). Εδώ οι οδηγίες συστήνουν σαφώς έναρξη καρδιοπροστατευτικής αγωγής, αν δε χορηγείται ήδη. Προχωρήσαμε λοιπόν σε τιτλοποίηση της δόσης των χορηγούμενων φαρμάκων και προσθήκη ροσουβαστατίνης, καθώς υπάρχουν αρκετά στοιχεία για την καρδιοπροστατευτική δράση των στατινών με αποτέλεσμα να προτείνεται η χρήση τους 20, 21. Από την άλλη, ενώ στο SPC του φαρμάκου προτείνεται διακοπή της τραστουζουμάμπης και επανεκτίμηση σε 3 εβδομάδες,16 αυτό δεν κρίνεται απολύτως απαραίτητο από τις επίσημες κατευθυντήριες οδηγίες, 20 καθώς πρόσφατες μικρές μελέτες δείχνουν ότι είτε δια-κοπεί είτε όχι το συγκεκριμένο φάρμακο, δεν υπάρχει διαφορά στο τελικό LVEF, αλλά και στα καρδιαγγειακά συμβάντα.22
Η παράλληλη και σχεδόν ταυτόχρονη μεταβολή του strain και των δύο κοιλιών που σημειώθηκε στην ασθενή αυτή, επιβεβαιώνει προηγούμενή μας μελέτη σε ασθενείς υπό τραστουζουμάμπη23 και υπογραμμίζει την αξία εκτίμησης και της δεξιάς κοιλίας με τους κλασικούς δείκτες, αλλά και με την επιμήκη παραμόρφωση του 24, 25. Αναφορικά με την αποκατάσταση του LVEF στους ασθενείς υπό τραστουζουμάμπη που εμφανίζουν συστολική δυσλειτουργία της αριστερής κοιλίας, το 20% δεν πρόκειται να το αποκαταστήσει, ενώ μόνο το 11% των ασθενών θα αποκαταστήσει πλήρως το LVEF.26 Η ασθενής που παρουσιάσαμε εδώ, δεν κατέστη δυνατό να αποκαταστήσει το LVEF στα αρχικά επίπεδα (αρχικό LVEF 62%, τελικό LVEF 50%), παρά το γεγονός ότι έλαβε θεραπεία καρδιακής ανεπάρκειας. Οι παράγοντες που προβλέπουν τη μη-αποκατάσταση του LVEF είναι η μεγαλύτερη αριστερή κοιλία (LVEDD >55mm και LVESD >40mm), το επηρεασμένο αρχικά LVEF (<50%), η πνευμονική υπέρταση (RVSP> 35mmHg) και η αναιμία. 26 Η πρόγνωση των ασθενών που δεν καταφέρνουν να αποκαταστήσουν το LVEF είναι χειρότερη και συσχετίζεται με υψηλότερη συχνότητα καρδιαγγειακών επεισοδίων.26
Τέλος, ένα σημαντικό ζήτημα που αφορά τη διαχείριση των ασθενών με καρδιοτοξικότητα από τραστουζουμάμπη είναι το χρονικό διάστημα για το οποίο θα πρέπει να συνεχίζουν να λαμβάνουν την αγωγή για καρδιακή ανεπάρκεια μετά την ολοκλήρωση της θεραπείας τους για τη νεοπλασία. Οι κατευθυντήριες οδηγίες συνιστούν την επ’ αόριστον χορήγηση της αγωγής, καθώς η διακοπή της ενδεχομένως να αυξήσει τον κίνδυνο για καρδιαγγειακά επεισόδια.20, 27, 28 Μελέτες έχουν δείξει ότι η τραστουζουμάμπη όταν χορηγείται μετά τη θεραπεία με ανθρακυκλίνες, συσχετίζεται με διπλάσιο κίνδυνο εμφάνισης καρδιακής ανεπάρκειας 9 χρόνια μετά τη θεραπεία συγκριτικά με ασθενείς που έχουν λάβει μόνο ανθρακυκλίνες, αλλά δεν υπάρχουν δεδομένα πιο μακροχρόνιας παρακολούθησης.29
Συμπέρασμα
Στόχος της καρδιο-ογκολογίας είναι η προστασία του καρδιαγγειακού συστήματος των ασθενών με νεοπλασία, εξασφαλίζοντας ότι θα λάβουν την καλύτερη δυνατή για τη νόσο τους θεραπεία που θα βελτιώσει την πρόγνωσή τους. Για να εξασφαλιστεί αυτό, πρέπει να υπάρχει καλή γνώση των ογκολογικών φαρμάκων, της επικείμενης καρδιοτοξικότητας με την οποία σχετίζονται και των σύγχρονων κατευθυντήριων οδηγιών, αλλά και υψηλός δείκτης κλινικής υποψίας, ακόμα και σε ασθενείς μέτριου κινδύνου για την έγκαιρη αναγνώριση και αντιμετώπιση των καρδιοτοξικών επιπλοκών.
Βιβλιογραφία
- ttps://www.wcrf.org/dietandcancer/cancer-trends/worldwide-cancer-data.
- Mohan N, Jiang J, Dokmanovic M and Wu WJ. Trastuzumab-mediated cardiotoxicity: current understanding, challenges, and frontiers. Antib Ther. 2018;1:13-17.
- Seshadri R, Firgaira FA, Horsfall DJ, McCaul K, Setlur V and Kitchen P. Clinical significance of HER-2/neu oncogene amplification in primary breast cancer. The South Australian Breast Cancer Study Group. Journal of clinical oncology : official journal of the American Society of Clinical Oncology. 1993;11:1936-42.
- Piccart-Gebhart MJ, Procter M, Leyland-Jones B, Goldhirsch A, Untch M, Smith I, Gianni L, Baselga J, Bell R, Jackisch C, Cameron D, Dowsett M, Barrios CH, Steger G, Huang CS, Andersson M, Inbar M, Lichinitser M, Láng I, Nitz U, Iwata H, Thomssen C, Lohrisch C, Suter TM, Rüschoff J, Suto T, Greatorex V, Ward C, Straehle C, McFadden E, Dolci MS and Gelber RD. Trastuzumab after adjuvant chemotherapy in HER2-positive breast cancer. The New England journal of medicine. 2005;353:1659-72.
- Romond EH, Perez EA, Bryant J, Suman VJ, Geyer CE, Jr., Davidson NE, Tan-Chiu E, Martino S, Paik S, Kaufman PA, Swain SM, Pisansky TM, Fehrenbacher L, Kutteh LA, Vogel VG, Visscher DW, Yothers G, Jenkins RB, Brown AM, Dakhil SR, Mamounas EP, Lingle WL, Klein PM, Ingle JN and Wolmark N. Trastuzumab plus adjuvant chemotherapy for operable HER2-positive breast cancer. The New England journal of medicine. 2005;353:1673-84.
- Farmakis D, Keramida K and Filippatos G. How to build a cardio-oncology service? European journal of heart failure. 2018;20:1732-1734.
- Moja L, Tagliabue L, Balduzzi S, Parmelli E, Pistotti V, Guarneri V and D’Amico R. Trastuzumab containing regimens for early breast cancer. The Cochrane database of systematic reviews. 2012;2012:Cd006243.
- Seidman A, Hudis C, Pierri MK, Shak S, Paton V, Ashby M, Murphy M, Stewart SJ and Keefe D. Cardiac dysfunction in the trastuzumab clinical trials experience. Journal of clinical oncology : official journal of the American Society of Clinical Oncology. 2002;20:1215-21.
- Farolfi A, Melegari E, Aquilina M, Scarpi E, Ibrahim T, Maltoni R, Sarti S, Cecconetto L, Pietri E, Ferrario C, Fedeli A, Faedi M, Nanni O, Frassineti GL, Amadori D and Rocca A. Trastuzumab-induced cardiotoxicity in early breast cancer patients: a retrospective study of possible risk and protective factors. Heart (British Cardiac Society). 2013;99:634-9.
- Slamon DJ, Leyland-Jones B, Shak S, Fuchs H, Paton V, Bajamonde A, Fleming T, Eiermann W, Wolter J, Pegram M, Baselga J and Norton L. Use of chemotherapy plus a monoclonal antibody against HER2 for metastatic breast cancer that overexpresses HER2. The New England journal of medicine. 2001;344:783-92.
- Procter M, Suter TM, de Azambuja E, Dafni U, van Dooren V, Muehlbauer S, Climent MA, Rechberger E, Liu WT, Toi M, Coombes RC, Dodwell D, Pagani O, Madrid J, Hall M, Chen SC, Focan C, Muschol M, van Veldhuisen DJ and Piccart-Gebhart MJ. Longer-term assessment of trastuzumab-related cardiac adverse events in the Herceptin Adjuvant (HERA) trial. Journal of clinical oncology : official journal of the American Society of Clinical Oncology. 2010;28:3422-8.
- de Azambuja E, Bedard PL, Suter T and Piccart-Gebhart M. Cardiac toxicity with anti-HER-2 therapies: what have we learned so far? Targeted oncology. 2009;4:77-88.
- El-Sherbeny WS, Sabry NM and Sharbay RM. Prediction of trastuzumab-induced cardiotoxicity in breast cancer patients receiving anthracycline-based chemotherapy. Journal of echocardiography. 2019;17:76-83.
- de Barros MVL, Macedo AVS, Sarvari SI, Faleiros MH, Felipe PT, Silva JLP and Edvardsen T. Left Ventricular Regional Wall Motion Abnormality is a Strong Predictor of Cardiotoxicity in Breast Cancer Patients Undergoing Chemotherapy. Arquivos brasileiros de cardiologia. 2019;112:50-56.
- Sato A, Yoshihisa A, Miyata-Tatsumi M, Oikawa M, Kobayashi A, Ishida T, Ohtake T and Takeishi Y. Valvular heart disease as a possible predictor of trastuzumab-induced cardioto-xicity in patients with breast cancer. Molecular and clinical oncology. 2019;10:37-42.
- https://www.ema.europa.eu/en/documents/product-information/herceptin-epar-product-information_en.pdf.
- Sawaya H, Sebag IA, Plana JC, Januzzi JL, Ky B, Tan TC, Cohen V, Banchs J, Carver JR, Wiegers SE, Martin RP, Picard MH, Gerszten RE, Halpern EF, Passeri J, Kuter I and Scherrer-Crosbie M. Assessment of echocardiography and biomarkers for the extended prediction of cardiotoxicity in patients treated with anthracyclines, taxanes, and trastuzumab. Circulation Cardiovascular imaging. 2012;5:596-603.
- Fallah-Rad N, Walker JR, Wassef A, Lytwyn M, Bohonis S, Fang T, Tian G, Kirkpatrick ID, Singal PK, Krahn M, Grenier D and Jassal DS. The utility of cardiac biomarkers, tissue velocity and strain imaging, and cardiac magnetic resonance imaging in predicting early left ventricular dysfunction in patients with human epidermal growth factor receptor II-positive breast cancer treated with adjuvant trastuzumab therapy. Journal of the American College of Cardiology. 2011;57:2263-70.
- Jones AL, Barlow M, Barrett-Lee PJ, Canney PA, Gilmour IM, Robb SD, Plummer CJ, Wardley AM and Verrill MW. Management of cardiac health in trastuzumab-treated patients with breast cancer: updated United Kingdom National Cancer Research Institute recommendations for monitoring. British journal of cancer. 2009;100:684-92.
- Curigliano G, Lenihan D, Fradley M, Ganatra S, Barac A, Blaes A, Herrmann J, Porter C, Lyon AR, Lancellotti P, Patel A, DeCara J, Mitchell J, Harrison E, Moslehi J, Witteles R, Calabro MG, Orecchia R, de Azambuja E, Zamorano JL, Krone R, Iakobishvili Z, Carver J, Armenian S, Ky B, Cardinale D, Cipolla CM, Dent S and Jordan K. Management of cardiac disease in cancer patients throughout oncological treatment: ESMO consensus recommendations. Annals of oncology : official journal of the European Society for Medical Oncology. 2020;31:171-190.
- Herrmann J LA, Sandhu NP, Villarraga HR, Mulvagh SL, Kohli M. Evaluation and management of patients with heart disease and cancer: cardio-oncology. . Mayo Clin Proc 2014;89(9):1287–1306
- Hussain Y, Drill E, Dang CT, Liu JE, Steingart RM and Yu AF. Cardiac outcomes of trastuzumab therapy in patients with HER2-positive breast cancer and reduced left ventricular ejection fraction. Breast cancer research and treatment. 2019;175:239-246.
- Keramida K, Farmakis D, Bingcang J, Sulemane S, Sutherland S, Bingcang RA, Ramachandran K, Tzavara C, Charalampopoulos G, Filippiadis D, Kouris N and Nihoyannopoulos P. Longitudinal changes of right ventricular deformation mechanics during trastuzumab therapy in breast cancer patients. European journal of heart failure. 2019;21:529-535.
- Keramida K and Farmakis D. Right ventricular involvement in cancer therapy-related cardiotoxicity: the emerging role of strain echocardiography. Heart failure reviews. 2020.
- Plana JC, Galderisi M, Barac A, Ewer MS, Ky B, Scherrer-Crosbie M, Ganame J, Sebag IA, Agler DA, Badano LP, Banchs J, Cardinale D, Carver J, Cerqueira M, DeCara JM, Edvardsen T, Flamm SD, Force T, Griffin BP, Jerusalem G, Liu JE, Magalhães A, Marwick T, Sanchez LY, Sicari R, Villarraga HR and Lancellotti P. Expert consensus for multimodality imaging evaluation of adult patients during and after cancer therapy: a report from the American Society of Echocardiography and the European Association of Cardiovascular Imaging. European heart journal cardiovascular Imaging. 2014;15:1063-93.
- Yoon HJ, Kim KH, Kim HY, Park H, Cho JY, Hong YJ, Park HW, Kim JH, Ahn Y, Jeong MH, Cho JG and Park JC. Impacts of non-recovery of trastuzumab-induced cardiomyopathy on clinical outcomes in patients with breast cancer. Clinical research in cardiology : official journal of the German Cardiac Society. 2019;108:892-900.
- Narayan HK, Finkelman B, French B, Plappert T, Hyman D, Smith AM, Margulies KB and Ky B. Detailed Echocardiographic Phenotyping in Breast Cancer Patients: Associations With Ejection Fraction Decline, Recovery, and Heart Failure Symptoms Over 3 Years of Follow-Up. Circulation. 2017;135:1397-1412.
- Telli ML, Hunt SA, Carlson RW and Guardino AE. Trastuzumab-related cardiotoxicity: calling into question the concept of reversibility. Journal of clinical oncology : official journal of the American Society of Clinical Oncology. 2007;25:3525-33.
- Banke A, Fosbøl EL, Ewertz M, Videbæk L, Dahl JS, Poulsen MK, Cold S, Jensen MB, Gislason GH, Schou M and Møller JE. Long-Term Risk of Heart Failure in Breast Cancer Patients After Adjuvant Chemotherapy With or Without Trastuzumab. JACC Heart failure. 2019;7:217-224
Επιμέλεια-Συγγραφή: ΚΑΛΛΙΟΠΗ ΚΕΡΑΜΙΔΑ1, ΜΑΡΙΑ ΑΝΑΣΤΑΣΙΟΥ2, ΠΑΝΑΓΙΩΤΑ ΟΙΚΟΝΟΜΟΠΟΥΛΟΥ2, ΙΓΝΑΤΙΟΣ ΟΙΚΟΝΟ-ΜΙΔΗΣ1, ΑΜΑΝΤΑ ΨΥΡΡΗ2, ΕΥΣΤΑΘΙΟΣ Κ. ΗΛΙΟΔΡΟΜΙΤΗΣ1, ΓΕΡΑΣΙΜΟΣ ΦΙΛΙΠΠΑΤΟΣ1
1 Ιατρείο Καρδιο-ογκολογίας, Μονάδα Καρδιακής Ανεπάρκειας, Β’ Πανεπιστημιακή Καρδιολογική Κλι-νική, Νοσοκομείο Αττικόν
2 Ογκολογικό Τμήμα, Β’ Προπαιδευτική Παθολογική Κλινική , Νοσοκομείο Αττικόν
Λέξεις Ευρετηρίου: καρκίνος μαστού, καρδιοτοξικότητα, τραστουζουμάμπη, επιμήκης παραμόρφωση του μυο-καρδίου (strain), καρδιακή ανεπάρκεια
Υπεύθυνος Επικοινωνίας: Καλιόπη Κεραμιδά,Ακαδημαϊκή Υπότροφος,Ιατρείο Καρδιο-ογκολογίας, Μονάδα Καρδιακής Ανεπάρκειας,Β’ Πανεπιστημιακή Καρδιολογική Κλινική, Νοσοκομείο Αττικόν
